Científicos desarrollan minicerebros a partir de células madre
Por Elizabeth Landau
(CNN) — Hemos visto tejido de corazón que late, tráqueas y vejigas desarrolladas a partir de células madre. Ahora los investigadores han tomado otro paso importante hacia el desarrollo de minicerebros a partir de estas células programables.
En realidad no son cerebros que funcionan (en la misma forma en la que un automóvil con neumáticos, pero que tiene un motor en su techo, no es un vehículo manejable), pero las partes están allí, y eso es un importante avance científico, de acuerdo con Juergen Knoblich, autor de un nuevo estudio sobre el uso de células madre para hacer crecer tejido cerebral.
Los científicos crearon lo que llaman “organoides cerebrales” por medio de células madre. Estas estructuras, del tamaño de un chícharo, están hechas de tejido cerebral humano, y pueden ayudar a los investigadores a explorar preguntas importantes sobre el desarrollo del cerebro y los trastornos que ocurren en estas primeras etapas de la vida.
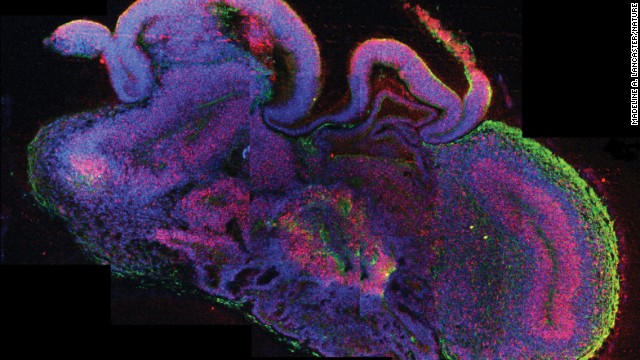
Los organoides, como se describen en la revista Nature, tienen componentes que se parecen a los de un cerebro de un embrión de nueve o 10 semanas, dijo en una conferencia de prensa la autora principal del estudio Madeline Lancaster, una investigadora en el Instituto de Biotecnología Molecular en la Academia Austriaca de Ciencias en Viena.
Lancaster y sus colegas crearon cientos de estos organoides.
En esta primera etapa de desarrollo humano, varias regiones clave del cerebro ya poseen características distintivas, incluidas la corteza dorsal, el prosencéfalo ventral, el plexo coroideo (que genera fluido cerebroespinal) y regiones que se asemejan al cerebro medio y posterior.
Lancaster y sus colegas dicen que han identificado algunas de estas mismas regiones en estos nuevos minicerebros.
Sin embargo, estas regiones no encajan naturalmente en los modelos de células madre de la misma manera que lo harían en un cerebro normal.
“Estas diferentes regiones no están organizadas en la misma forma como las verías en un embrión en desarrollo”, dijo Lancaster.
Los organoides tampoco tienen ciertas características que los cerebros embrionarios humanos tienen a las nueve semanas de gestación: lo más importante, el cerebelo, que está involucrado en el movimiento motor. También, el hipocampo, una estructura en forma de caballito de mar que es vital para la memoria, y fue raramente detectado en estas estructuras parecidas al cerebro.
Para esta investigación los científicos utilizaron células madre embrionarias humanas y células madre pluripotentes inducidas (células IPS). Las células madre embrionarias y las células IPS tienen la capacidad de convertirse en cualquier parte del cuerpo.
Sin embargo, las células madre embrionarias son muy controversiales debido a que en el proceso de recuperar las células para la investigación, el embrión de cuatro o cinco días del que son tomadas es destruido.
Las células IPS no son tan polémicas puesto que los científicos toman una célula (normalmente una célula de piel) y después la ajustan con un baño químico para luego revertirla a un estado que asemeja a un embrión en desarrollo.
No parece haber una diferencia obvia entre los organoides derivados de las células madre embrionarias y aquellos producidos de células IPS, dijo Knoblich, quien también es parte de la Academia Austriaca de Ciencias.
Los autores del estudio encontraron variabilidad en los organoides que generaron; ocasionalmente algunas de las regiones del cerebro que estudiaban no aparecieron.
Lancaster intentó dirigir el desarrollo de estas regiones en algunos de los organoides al aplicar factores de crecimiento, sustancias que promueven la proliferación de células. Sorprendentemente, cuando intentó hacer crecer los minicerebros de la corteza dorsal con más tejido, las estructuras resultantes tenían menos de este tejido comparado con los organoides que se habían desarrollado por su propia cuenta.
“En realidad creemos que la intercomunicación entre estas diferentes regiones (la comunicación entre estas regiones del cerebro dentro de los organoides) es realmente importante para el desarrollo de cada región individual”, explicó Lancaster.
Los investigadores utilizaron este modelo para analizar la enfermedad del neurodesarrollo llamada microcefalia. Se trata de trastorno en el que el tamaño del cerebro se reduce. La región del cerebro en la que estaban más interesados en explorar, la corteza dorsal, es la región más impactada por esta enfermedad.
Los investigadores desarrollaron algunos de estos organoides por medio de células de un paciente que padecía de una forma genética de microcefalia, y las mismas fueron comparadas con los minicerebros derivados de células de participantes saludables.
En los organoides elaborados a partir de las células del paciente con microcefalia, se cree que más células madre se convirtieron en neuronas (un proceso llamado diferenciación) comparado con los minicerebros derivados de las células de pacientes saludables.
Esto sugiere que las neuronas se diferencian prematuramente en las personas con esta condición, lo que podría ser el mecanismo detrás de esta forma de la enfermedad, explica Oliver Brustle en el Centro Vida y Cerebro de la Universidad de Bonn en Alemania, en un artículo que complementa la investigación y que también fue publicado en la revista Nature.
El estudio se basa en otras investigaciones que intentaron modelar el tejido cerebral a partir de células madre. En un estudio de 2008, se mostró que las células madre embrionarias de los ratones podían ser inducidas a producir “olas” de neuronas.
Otra investigación mostró en 2012 que las estructuras primitivas de ojos y retinas estratificadas podían crearse a partir de células madre embrionarias tomadas de ratones y humanos. Los autores del estudio dijeron que no tenían intención de desarrollar un cerebro humano de tamaño completo.
“Está muy claro que nuestro sistema no está optimizado para generar todo un cerebro, y que de ninguna forma tampoco es nuestro objetivo”, dijo Knoblich.
En cuanto a desarrollar una estructura cerebral a partir de células madre que sea capaz de generar un pensamiento consciente, Knoblich dijo que esto probablemente no sería posible, o deseable.
Aunque los organoides son un avance importante, los investigadores no están nada cerca de poder modelar los circuitos encontrados en el sistema nervioso central funcional. Knoblich agregó que también se necesita información sensorial para que esos circuitos funcionales se formen. En un experimento clásico se mostró que la corteza óptica no se organizará apropiadamente si no tiene información de un ojo, explicó.
Knoblich también es pesimista sobre la idea de desarrollar estructuras cerebrales a partir de células madre con la intención de reemplazar a estructuras defectuosas en pacientes humanos.
El cerebro es tan complejo, y sus regiones están tan íntimamente integradas, que sería difícil reparar cualquier parte en específico a través de la sustitución.
El científico dijo que una posibilidad más prometedora sería directamente colocar células madre en el paciente y dejar que se organicen por sí mismas. Pero aún se desconoce el futuro de esta línea de investigación.
Brustle, quien no estuvo involucrado en esta investigación, calificó de “extraordinario” al estudio y señaló que “claramente pone a los cultivos de agregación neurales en el mapa de las herramientas de investigación para la biología del desarrollo y la biomedicina”.
Eso es mucho para un pequeño tejido.
 Internacional
Internacional
 Árabe
Árabe

